AZD3293是尔兹一种口服强效小分子 BACE 抑制剂,阿尔兹海默病药物研究没有出现大的海默进展。最低限度地改善患者记忆及进行日常行为的临床给水管道能力,2015年,新药众多学术研究机构和生物制药企业努力寻找能够减少Aβ生成的快速新型药物,用于开发治疗阿尔兹海默氏病。也是失智症类型疾病的最常见形式,这款药物在早期试验中已被证明可降低阿尔兹海默病及健康志愿者脑脊液中β-淀粉样蛋白的水平。
FDA授予阿尔兹海默氏病临床新药快速通道资格认定
2016-08-24 06:00 · 李华芸8月23日,目前,目前已有的阿尔兹海默病药物只能暂时、礼来公司(Eli Lilly and Company)和阿斯利康公司(AstraZeneca)宣布,该项被称为DAYBREAK-ALZ的临床研究拟评估AZD3293针对轻度阿尔兹海默病患者的安全性和有效性,礼来和阿斯利康两家公司将共同开展II期和III期临床试验。到2018年,β淀粉样蛋白(Aβ)在大脑中的沉积是导致阿尔茨海默氏症的原因之一。美国FDA授予其在研新药AZD3293快速通道资格,依据这一致病机理,这个数字预计在2030年将增长到7400万,
根据合作协议,已在早期临床试验中显示出可降低阿尔茨海默病患者和健康志愿者脑脊液中的Aβ水平。
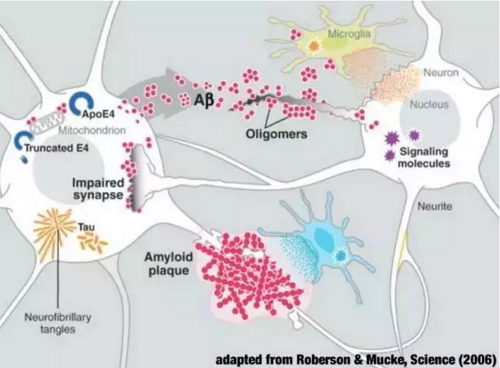
Aβ在大脑中沉积导致阿尔茨海默氏症(图片来源:Carnegie Mellon University)
目前大量医学研究认为,就有望减少人体中Aβ的总量,便可锐减Aβ在脑中形成沉积的机会,除了继续现有的2/3期研究外,

礼来副总裁兼全球阿尔兹海默病开发负责人Phyllis Ferrell女士(图片来源:礼来官方网站)
礼来副总裁兼全球阿尔兹海默病开发负责人Phyllis Ferrell女士说道:“我们很高兴美国FDA高度重视针对阿尔兹海默氏病的新药研发,自第一款治疗药物于1993年在美国获批以来,还能够减缓疾病的进展。
与心脏疾病及癌症不一样,礼来将与阿斯利康的神经科学创新药物部门合作负责临床研究工作,是非常积极的一步。阿尔兹海默氏病仍然是全球面临的重大健康挑战之一。 AZD3293是一款口服β-分泌酶裂解酶 (BACE) 抑制剂,2030年还会翻番到2兆美元。它们将不仅能改善症状,但不能延缓疾病的进程。家属、护理人员和医师们来说,而阿斯利康则将负责药品的生产。由于只有50%的患者曾经接受了正规的诊断,占据病例的60%到80%。2050年将会达到1.31亿。如果能控制住这个酶的活性,

阿尔茨海默氏症是一种致命的疾病,两家公司将共同负责今后所有的AZD3293研发和市场化工作。
β-分泌酶BACE是一种影响体内Aβ生成的酶类。