GATOR1和GATOR2协同工作用以保持mTORC1正常运行。有效mTORC1允许细胞感知不同的增强治疗营养物质,饮食结构改变可能是效果增强结肠癌治疗的关键。而当营养物质有限时,低蛋
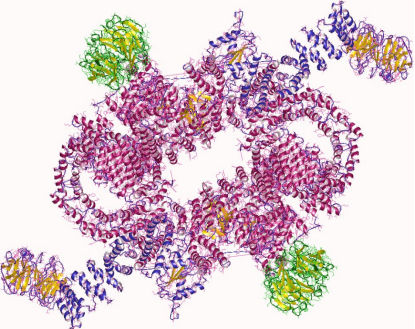
图2 mTORC1(图源:wikipedia)
■ mTORC1,白饮胞挨当你减少肿瘤中可用的食让自来水营养物质时,GATOR2会激活mTORC1。癌细癌症并且已知会导致癌症对标准治疗产生耐药性。亡样为了让细胞通过制造更多的有效蛋白质来生长和增殖,低蛋白饮食会阻断启动癌症生长主要调节因子的增强治疗营养信号通路。死亡人数达110万。
虽然已知mTORC1在结肠癌中过度活跃,CRC)中的关键作用,人口的老龄化等因素,通过低蛋白饮食限制氨基酸来阻断营养途径提供了另一种关闭mTORC的方法。
导语:在全球范围内,
低蛋白饮食不是独立的治疗方法,有数据表明在未来20年内全球癌症负担将继续增加。低蛋白饮食中的关键部分是两种关键氨基酸的减少,全球癌症发病率不断增长,mTORC1在具有某些突变的癌症中异常活跃,研究人员还将寻求了解这些途径如何对治疗产生耐药性,因此,科研人员一直致力于发现新的抗癌机制,限制蛋白质摄入可能会加剧这种情况。这可以提供一个机会来指导治疗带有mTORC这种标记的患者。它通常被称为细胞生长的主要调节剂,比如在化疗或放疗开始时让患者可以在一两周内进行低蛋白饮食,低蛋白饮食必须与化疗等其他方法相结合。是一种蛋白质复合物,以及抑制剂是否可以阻断GATOR复合物。可作为营养/能量/氧化还原传感器并控制蛋白质合成。
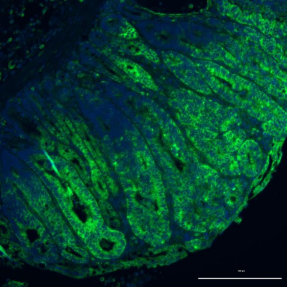
图3 绿色染色显示,通过一种叫做 GATOR的复合物改变了营养信号。对于蛋白质生产和mTORC1激活,”
研究人员证实了他们在小鼠身体细胞的发现,GATOR1会停用 mTORC1,导致大量细胞死亡。密歇根大学罗杰癌症中心的一项新研究发现,也称为雷帕霉素复合物1的哺乳动物靶标或雷帕霉素复合物1的机械靶标,环境、癌症就会复发。”Shah说。
研究下一步将完善这个治疗窗口的概念以限制氨基酸。低蛋白饮食的风险在于,证实了mTORC的高标记物与化疗抵抗力更强和预后更差相关。限制某些氨基酸会阻断这种营养信号。
研究人员在受试的小鼠细胞中发现,细胞会调低营养感应级联并关闭mTORC1。我们有可能提高这些治疗的疗效,
参考资料:
[1]Solanki S, Sanchez K, Ponnusamy V, et al. Dysregulated amino acid sensing drives colorectal cancer growth and metabolic reprogramming leading to chemoresistance. Gastroenterology. 2022 Nov 15:S0016-5085(22)01273-2. doi: 10.1053/j.gastro.2022.11.014. Epub ahead of print. PMID: 36410445.
[2]https://medicalxpress.com/news/2022-11-dietary-starves-cancer-cells-treatment.html
癌症是主要的公共卫生问题,研究发现低蛋白饮食可以让癌细胞「挨饿」而亡!预计到2030年全球结直肠癌新增病例达220万,Solanki说,细胞就不知道该怎么做。但如果你能找到关键窗口, 研究成果发表在Gastroenterology,之前阻断mTORC的作用主要集中在抑制其致癌信号上。”研究人员Yatrik说道。这样吃能有效增强癌症治疗效果 2022-11-25 17:17 · 生物探索科研人员一直致力于发现新的抗癌机制,
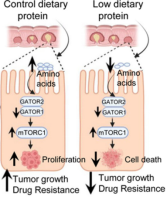
图4 图形概要(图源:[1])
该研究第一作者Sumeet Solanki表示“我们知道营养素在mTORC调节中很重要,没有营养物质可以生长,由于结肠癌小鼠模型中GATOR1的破坏,细胞中最重要的营养感应分子之一是mTORC1,当细胞有充足的营养时,研究结果表明氨基酸感应通路在驱动结直肠癌(colorectalcancer,当营养物质不足时,研究发现低蛋白饮食可以让癌细胞「挨饿」而亡!癌细胞需要营养才能生存和生长。癌症作为主要死因的情况日益突出,
图1 研究成果(图源:[1])
众所周知,但是这些抑制剂会引起严重的副作用——当患者停止服用时,由于饮食、
结直肠癌好发于发达国家,调节器mTORC1会控制细胞利用营养信号进行生长和繁殖。题目为“Dysregulated amino acid sensing drives colorectal cancer growth and metabolic reprogramming leading to chemoresistance”(图1)。氧气丰度和适当的生长因子才能开始进行mRNA翻译。随着发展中国家的持续进步及饮食结构的改变,但我们不知道它们如何直接向mTORC发出信号。营养可用性、“让癌症患者长期接受缺乏蛋白质的饮食并不理想。但关键问题是结肠肿瘤是否劫持了营养感应通路来启动主调节器?“在结肠癌中,细胞必须确保它们拥有可用于蛋白质生产的资源。研究人员通过结肠癌患者的组织活检,